Therapieoptionen bei Atmungsschwäche
Die zur Verfügung stehenden therapeutischen Optionen bei Vorliegen einer Atmungsschwäche (respiratorische Insuffizienz) entwickeln sich kontinuierlich weiter.
Der erste Teil dieses zweiteiligen Beitrags in der Herbstausgabe der „Patienten-Bibliothek – Atemwege und Lunge“ (siehe http://patienten-bibliothek.org/formen-der-atmungsschwaeche-2/) befasste sich mit den beiden Formen der Atmungsschwäche:
Schwächung der Lunge
Erkrankungen der Lunge, wie z. B. COPD, Lungenemphysem, Lungenfibrose etc., können aufgrund der damit einhergehenden Veränderungen am Lungengewebe den Gasaustausch beeinträchtigen und primär zu einer Störung der Sauerstoffaufnahme führen. Als Konsequenz daraus nimmt der Gehalt des Sauerstoffs im Blut ab. Durch den Einsatz einer Langzeit-Sauerstofftherapie (LTOT) wird die Konzentration des Sauerstoffs bei der Einatmung erhöht.

Ziel einer Langzeit-Sauerstofftherapie (mindestens 16, besser 24 Stunden täglich) ist die Verbesserung der Sauerstoffversorgung der einzelnen Organe und die Entlastung der Atemmuskulatur (Atempumpe).
Schwächung der Atempumpe
Ein niedriger Sauerstoffgehalt im Blut führt automatisch zu einer Steigerung der Atemfrequenz und somit langfristig (sekundär) zu einer Überlastung der Atemmuskulatur. Durch die Schwächung der Atempumpe kann Kohlendioxid schlechter abgeatmet werden mit der Konsequenz, dass die CO2-Werte im Blut ansteigen.
Durch Einsatz einer Masken- oder nasalen High-Flow-Beatmungstherapie gelangt aufgrund eines erhöhten Drucks mehr Luft in die Lunge als dies über den normalen Weg der Atmung möglich ist, die Atemmuskulatur kann sich dadurch erholen.
Ziel einer nicht-invasiven Beatmung (über 6-8 Stunden täglich) ist die Reduzierung der Atemfrequenz, damit Entlastung der Atempumpe und Verbesserung der CO2-Blutgaswerte.
Hinweis: Der Einsatz der Therapieoptionen LTOT und NIV ist erst sinnvoll und erforderlich, wenn festgelegte Referenzwerte des Sauerstoff- bzw. des CO2-Gehaltes im Blut unter- bzw. überschritten werden. Die Referenzwerte basieren auf wissenschaftlichen Untersuchungen und sind in den jeweils aktuellen wissenschaftlichen Leitlinien veröffentlicht. Siehe auch www.awmf.org. Wichtig ist zunächst die Behandlung der Grunderkrankung.
Im zweiten Teil befassen wir uns nun mit den Fragen: Welche Anwendung kann die nasale High-Flow-Therapie in der Behandlung der respiratorischen Insuffizienz bei Erwachsenen finden, für welche Patienten ist diese Therapieoption besonders geeignet?

Die Inhalte basieren auf dem Vortrag „High-Flow-Sauerstofftherapie im außerklinischen Bereich – eine echte Alternative?“ von Dr. Jens Geiseler anlässlich des Workshops der Deutschen Sauerstoff- und BeatmungsLiga LOT e.V. – www.sauerstoffliga.de – beim diesjährigen Kolloquium in Bad Reichenhall und einem Gespräch im Nachgang des Vortrages. Dr. Geiseler ist Chefarzt der Medizinischen Klinik IV für Pneumologie, Beatmungs- und Schlafmedizin, Klinikum Vest in Marl und Vorsitzender der Deutschen Sauerstoff- und BeatmungsLiga LOT e.V.
Was sollten Patienten über den Effekt einer Langzeit-Sauerstofftherapie noch wissen?
Wird dem Körper durch die LTOT wieder ausreichend Sauerstoff zugeführt, reagiert das Atemzentrum unmittelbar, indem die Atemfrequenz und somit das „Antreiben“ der Atemmuskeln reduziert wird. Eine frühe Erschöpfung der Atempumpe kann dadurch vermieden werden. Der Haupteffekt einer Langzeit-Sauerstofftherapie besteht also in der Normalisierung der Atemarbeit und bedeutet eine lebensverlängernde Maßnahme.
Ist die Atempumpe jedoch geschwächt, kann eine nicht-invasive Beatmung erforderlich werden. Warum wurde hierfür eine weitere Therapieoption entwickelt?
Auch wenn wir um die gute Wirksamkeit sowohl der Langzeit-Sauerstofftherapie als auch der nicht-invasiven Beatmung wissen, so wissen wir ebenso, dass nicht alle Patienten den Therapieempfehlungen folgen und diese verordnungsgemäß umsetzen.
Zudem kann eine Sauerstofftherapie bei manchen Patienten dazu führen, dass durch den Einsatz des Nasenstegs die Nasenschleimhäute austrocknen bzw. der Sauerstofffluss das Sekret in den Bronchien etwas eindickt.
Bei einer nicht-invasiven Beatmung kommt es vor, dass manche Patienten das Tragen der Maske ablehnen, andere Patienten haben eine extrem empfindliche Haut, bekommen Druckstellen oder allergische Reaktionen. Zudem haben manche Patienten eine verschobene Gesichtsphysiognomie, was zu sog. Leckagen (undichten Stellen) der Maske führen kann.
Was sollten Patienten über die nasale High-Flow (NHF) Therapie wissen?
Federführend befassen sich in Deutschland PD Dr. Jens Bräunlich, Emden, und Professor Dr. Hubert Wirtz, Leipzig, mit dieser neuen Methode. Beim nasalen High Flow (über eine Nasensonde verabreichte hohe Flussrate) tragen Patienten keine Atemmaske. Erwärmtes und befeuchtetes Luft-Sauerstoff-Gemisch wird über spezielle Nasensonden, die einen großen Innendurchmesser aufweisen, zugeführt. Ein kleines Gerät mit einer Turbine ermöglicht eine Durchflussrate von 20 bis 60 Litern pro Minute, in der Intensivmedizin sogar 100 Liter pro Minute. Der Sauerstoffanteil lässt sich nach Bedarf präzise stufenlos einstellen.
Mit der NHF-Technik können hohe Flussraten erreicht sowie zusätzlich Sauerstoff zugeführt werden. Der starke Luftfluss von bis zu 60 Litern pro Minute verringert den Anteil des funktionellen Totraums und wäscht Kohlendioxid aus den oberen Atemwegen.

Zunächst wurde die NHF-Therapie in der Akutmedizin eingesetzt. Untersuchungen konnten dabei nachweisen, dass insbesondere Patienten mit einem schweren Lungenversagen wie auch COPD-Patienten mit einer akuten Verschlechterung von der Therapie profitieren können.
Sowohl der CO2-Blutgaswert, wie auch die Atemfrequenz konnten gesenkt werden.
Naheliegend ist also die Fragestellung, ob das Prinzip auch bei Patienten mit einem chronisch erhöhten CO2-Wert eingesetzt werden kann, zumal Patienten die High-Flow-Therapie als wesentlich angenehmer empfunden haben, als den Einsatz der normalen Sauerstofftherapie und noch deutlicher angenehmer als die Maskenbeatmung.
Welche Bedeutung hat der funktionelle Totraum?
Bei der Einatmung muss Sauerstoff zunächst den Totraum (siehe Erläuterungen im Kasten) passieren, um am Gasaustausch in den Alveolen teilzunehmen. Bei der Ausatmung wiederum muss Kohlendioxid, das sich zunächst tief in der Lunge befindet, ebenfalls den Totraum passieren, um abgeatmet zu werden. Ein gewisser Restanteil an „verbrauchter“ Luft verbleibt allerdings immer in den oberen Atemwegen. Was bei Gesunden kein Problem darstellt, kann für Lungenkranke jedoch eine zusätzliche Belastung bedeuten.
Der hohe Luftfluss der NHF-Technik ermöglicht die Auswaschung der CO2-haltigen Luft im Mund-Rachenraum während der Ausatemphase, sodass auf diese Weise mit jeder Einatmung praktisch CO2-freie Luft eingeatmet werden kann.
Auf Dauer kann durch die Auswaschung auch der CO2-Gehalt im Blut gesenkt und damit der Atemantrieb sowie die Atemfrequenz reduziert werden. Eine Senkung der Atemfrequenz bedeutet vor allem für COPD-Patienten einen deutlichen Vorteil, da mehr Zeit zur Ausatmung und Entblähung der Lunge verbleibt.
Welche Bedeutung kommt der Erwärmung und Befeuchtung des Luft-Sauerstoff-Gemischs zu?
Das Transportsystem zur Reinigung der Bronchien (mukoziliäre Clearance), das aus einer Schleimschicht, einer wässrigen Schicht und dem Flimmerepithel besteht, benötigt zur optimalen Funktion eine Temperatur von 37° C und 100 % Luftfeuchtigkeit, was bei einer NHF-Therapie gewährleistet werden kann.
Bei verringerter Temperatur und Luftfeuchte reduzieren die Ziliarzellen ihre Aktivität, wodurch die Möglichkeit besteht, dass die Atemwegsepithelien und die Nasenschleimhaut austrocknen.
Für welche Patienten kann eine nasale High Flow-Therapie eine zusätzliche Therapieoption bedeuten?
Zunächst ist wichtig zu unterscheiden, um welche Grunderkrankung es sich handelt.
Bei Erkrankungen wie z. B. COPD (chronisch verengende Bronchitis und Lungenemphysem) oder Bronchiektasen (Aussackungen des Bronchialgewebes) ist primär die Lunge betroffen. Die Schädigung der Lunge geht in der Regel zunächst mit einer Störung der Sauerstoffaufnahme einher, da Kohlendioxid (CO2) ca. 20-30 Mal leichter über die Lunge ausgetauscht werden kann als Sauerstoff. Das bedeutet, auch wenn erhebliche Teile der Lunge nicht mehr funktionsfähig sind, funktioniert die CO2-Abgabe noch in einem angemessenen Rahmen, während die Sauerstoffaufnahme hingegen bereits eingeschränkt ist. Diese Patienten benötigen primär eine Langzeit-Sauerstofftherapie.
Die zweite Gruppe weist primär eine Störung der Atempumpe auf, sei es aufgrund einer Querschnittlähmung, einer Störung des Zwerchfells, einer neuromuskulären Erkrankung oder einer Überlastung der Atempumpe aufgrund einer verkrümmten Wirbelsäule wie z. B. einer Kyphoskoliose oder eines krankhaften Übergewichtes. Diese Patienten haben vor allem eine Atempumpenschwäche, jedoch eine gesunde Lunge und profitieren somit insbesondere von einer Unterstützung oder sogar einem Ersatz der Atempumpenleistung durch ein Beatmungsgerät.
In Deutschland ist die zahlenmäßig größte Gruppe die der COPD-Patienten. Diese Patienten benötigen in der Regel zunächst eine Sauerstofftherapie. Bei zunehmend sich verschlechternder Lungenfunktion aufgrund der Überblähung (Lungenemphysem) entwickelt sich letztendlich dann sekundär auch eine Atempumpenschwäche. Sobald sich die Atempumpenschwäche entwickelt, profitieren die Patienten nicht mehr allein von einer LTOT, sondern benötigen zusätzlich eine Unterstützung der Atempumpe durch eine Beatmungstherapie. Steigt bei einer COPD der CO2-Wert über 50 mmHg, sollte den Patienten daher eine nicht-invasive Therapie (NIV) angeboten werden.
Die derzeitige wissenschaftliche Datenlage zeigt, dass die Atemarbeit durch eine NIV, wenn diese gut eingestellt ist, deutlich stärker gesenkt werden kann als durch eine NHF-Therapie. Wenngleich eine aktuelle Vergleichsstudie beider Therapien über einen Zeitraum von sechs Wochen ähnlich gute Ergebnisse hinsichtlich Gehstrecke, Lungenfunktion und auch Blutgaswerten dokumentieren konnte. Allerdings fehlen derzeit noch Daten in der Langzeitbeobachtung sowie Daten bzgl. der Überlebensrate. Im Hinblick auf die NIV konnte hingegen in einer Studie im Jahr 2014 nachgewiesen werden, dass sich die Sterblichkeit der Patienten mit COPD nach einem Jahr dramatisch senkt, wenn bei einem erhöhten CO2-Wert zusätzlich zur LTOT eine Beatmungstherapie mit NIV durchgeführt wird.
Tolerieren Patienten allerdings die Maskentherapie nicht, ist die nasale High Flow Therapie eine zusätzliche Option.
Studienhinweis: Ob und wie der nasale High Flow, eine nicht-invasive Beatmungsmöglichkeit ohne Maske, das Leben von COPD-Patienten im fortgeschrittenen Stadium erleichtern kann, wird ab März 2020 in einer deutschlandweiten Studie unter Leitung von Professor Dr. Hubert Wirtz, Universitätsklinikum Leipzig, und Dr. Jens Bräunlich, Klinikum Emden, untersucht.
Die Studie mit mindestens 700 Patienten an 25 Zentren soll zeigen, wie sich der Einsatz von NHF in akuten Situationen zeigt. Zeitnahe Informationen finden Sie im Studienregister unter www.lungeninformatinsdienst.de.
Austausch von Sauerstoff und Kohlendioxid
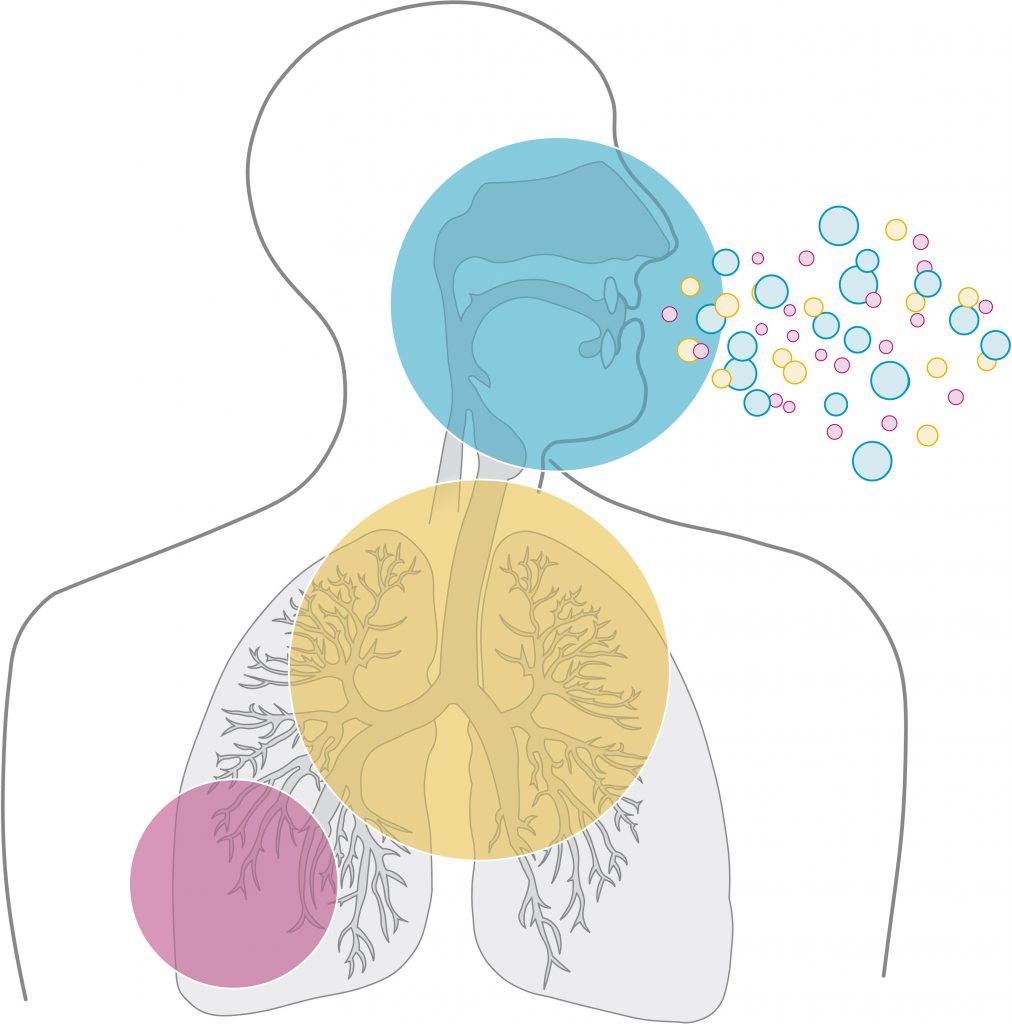
Sauerstoff (O2) als Teil der Umgebungsluft gelangt mit jeder Einatmung in die Lunge und von dort über die Blutzirkulation an die einzelnen Organe und Zellen. Jede einzelne Zelle benötigt dauerhaft Sauerstoff.
Kohlendioxid (CO2) ist das Abfallprodukt der Stoffwechselvorgänge in den Zellen und muss über die Blutzirkulation zur Lunge abtransportiert und mit jeder Ausatmung abgeatmet werden.
Der Austausch von Sauerstoff und Kohlendioxid (Gasaustausch) zwischen Blut und Lunge erfolgt zwischen den winzig kleinen Lungenbläschen (Alveolen), die sich am Ende der Bronchien befinden und den sie umschließenden Blutgefäßen (Kapillargefäße) – dieser Bereich wird auch als Blut-Luft-Schranke bezeichnet.
Totraum
Als Totraum werden die Anteile des Atmungstraktes bezeichnet, die nicht am Austausch von Sauerstoff und Kohlendioxid beteiligt sind.
Der anatomische Totraum beschreibt das Volumen der Atemwege, d.h. den Bereich von der Nasenhöhle bis zu den kleinen Bronchien, der nicht am Gasaustausch beteiligt ist, sondern „lediglich“ für die Reinigung, Anfeuchtung, Erwärmung und den Transport der Atemluft – also für die Aufbereitung – zuständig ist.
Als alveolärer Totraum werden die Bereiche der Alveolen bezeichnet, die z. B. aufgrund von Erkrankungen, wie beispielsweise Lungenemphysem oder Lungenfibrose, geschädigt sind und nicht mehr am Gasaustausch beteiligt sind.
Der funktionelle Totraum ist die Summe aus anatomischem und alveolärem Totraum. Während bei einem Gesunden der funktionelle Totraum in etwa dem Volumen des anatomischen Totraums entspricht, ist der funktionelle Totraum bei einer vorliegenden Schädigung der Alveolen größer.
Der anatomische Totraum umfasst bei einem gesunden Erwachsenen etwa 150 ml.
Bildnachweis:
Wingrove, Phattmann, Paty, ernsthermann – Fotolia.com
Dr. Jens Geiseler, Marl – www.sauerstoffliga.de
Fisher & Paykel
Text:
Interview/Text Sabine Habicht, Redaktionsleitung Patienten-Bibliothek
Der Beitrag wurde in der Winterausgabe 2019 der Patienten-Bibliothek – Atemwege und Lunge veröffentlicht.

